国家药监局提出探索实现30个工作日内完成创新药临床试验申请审评审批,旨在缩短药物临床试验启动时间,加快创新药研发速度。这一举措将加速突破性治疗品种的研发进程,为患者带来更快的治疗方案。
🚀 **加快创新药研发速度**: 国家药监局提出探索实现30个工作日内完成创新药临床试验申请审评审批,旨在缩短药物临床试验启动时间,加快创新药研发速度,为患者带来更快的治疗方案。
这一举措将加速突破性治疗品种的研发进程,为患者带来更快的治疗方案。突破性治疗品种是指针对严重疾病,且已在前期临床试验中显示疗效或安全性方面显著优于现有治疗手段的新药。
通过缩短审评审批时间,可以加快突破性治疗品种的上市速度,让更多患者受益于新药带来的治疗效果。
💊 **突破性治疗品种**: 突破性治疗品种名单是中国国家药品监督管理局药品审评中心 (CDE) 为加快开发针对严重疾病、且已在前期临床试验中显示疗效或安全性方面显著优于现有治疗手段的新药而设计的一种药品审评程序。
纳入突破性治疗品种名单的药物通常用于防治严重危及生命或严重影响生存质量的疾病,在现有治疗手段无效或相比具有明显临床优势时,可以获得 CDE 的快速雷评待遇,加快药物上市速度。
💡 **药物发现过程**: 药物发现是指一个新的候选药物的发现过程,它是一个漫长而复杂的过程,通常需要数年甚至数十年的时间。
药物发现过程包括以下几个关键步骤:
1. 药物靶点的识别和验证
2. 药物先导化合物的发现和优化
3. 药物候选化合物的筛选和评价
4. 临床前研究
5. 临床试验
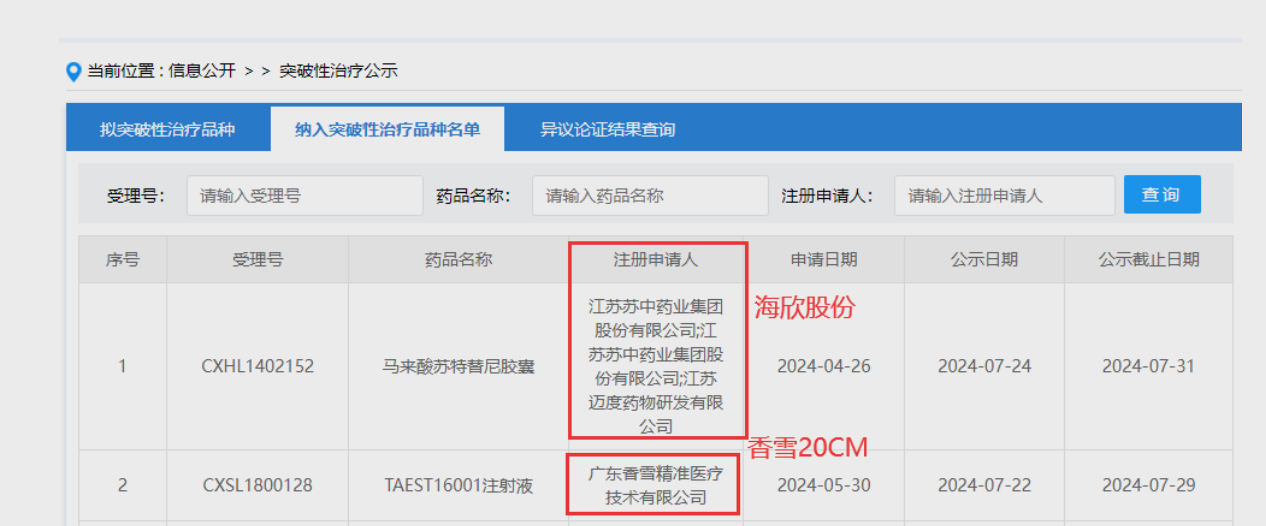
一、创新药对标! 8月1日,国家药监局提出,探索实现30个工作日内完成创新药临床试验申请审评审批,缩短药物临床试验启动用时药物发现是指一个新的候选药物的发现过程突破性治疗品种名单是中国国家药品监督管理局药品审评中心(CDE)为加快开发针对严重疾病、且已在前期临床试验中显示疗效或安全性方面显著优于现有治疗手段的新药而设计的一种药品审评程序。纳入突破性治疗品种名单的药物通常用于防治严重危及生命或严重影响生存质量的疾病,在现有治疗手段无效或相比具有明显临床优势时,可以获得CDE的快速雷评待遇,加快药物


