文章介绍了一项针对实体肿瘤中CD8+T细胞免疫逃逸问题的创新性解决方案。研究发现,肿瘤细胞线粒体是构建免疫抑制微环境的关键,其丰富程度与肿瘤的抵抗力成正比。中国科学院国家纳米科学中心团队开发的mitoNIDs纳米降解剂,通过“纳米诱导临近技术”,精准靶向癌细胞线粒体,诱导其进行选择性自噬降解。这一过程能显著提升CD8+T细胞的杀伤力,通过增加肿瘤细胞表面MHC-I分子、减少抗凋亡蛋白BCL-XL以及释放激活T细胞的信号分子溶血磷脂酰肌醇,从而增强免疫治疗效果。在动物模型中已显示出积极结果,未来有望应用于多种疾病领域。
🎯 肿瘤线粒体是免疫抑制的关键:实体肿瘤细胞的线粒体不仅支撑其代谢,还能通过多种机制构建免疫抑制微环境,削弱CD8+T细胞的抗肿瘤活性。线粒体越丰富的肿瘤细胞,抵抗免疫攻击的能力越强。
🔬 mitoNIDs纳米降解剂实现“线粒体自毁”:中国科学院国家纳米科学中心团队研发的mitoNIDs纳米降解剂,利用“纳米诱导临近技术”,将线粒体靶向肽和自噬相关蛋白LC3识别肽结合。该系统能引导癌细胞的线粒体与自噬系统靠近,触发选择性自噬降解,实现肿瘤细胞的“自毁”。
🚀 增强CD8+T细胞杀伤力:线粒体被降解后,肿瘤细胞的MHC-I分子表达增多,使其更容易被CD8+T细胞识别;同时,抗凋亡蛋白BCL-XL减少,增加癌细胞凋亡的易感性。此外,线粒体降解释放的溶血磷脂酰肌醇还能直接激活CD8+T细胞的活性,从而全面提升免疫治疗效果。
💡 临床应用前景广阔:在小动物肿瘤模型中,mitoNIDs与免疫疗法联用取得了显著的肿瘤抑制效果。该技术未来有望在临床试验中得到验证,并可能扩展应用于自身免疫病、神经退行性疾病等多种需要精准分子干预的疾病领域。
人类免疫系统中的CD8+T细胞本是清除异常细胞的“杀手锏”,却常在实体肿瘤面前“失灵”。关键原因在于肿瘤细胞的线粒体——这些“能量工厂”不仅支撑肿瘤代谢,还会构建免疫抑制微环境,通过抑制免疫信号、争夺营养等方式削弱免疫攻击,线粒体越丰富的肿瘤细胞抵抗力越强。
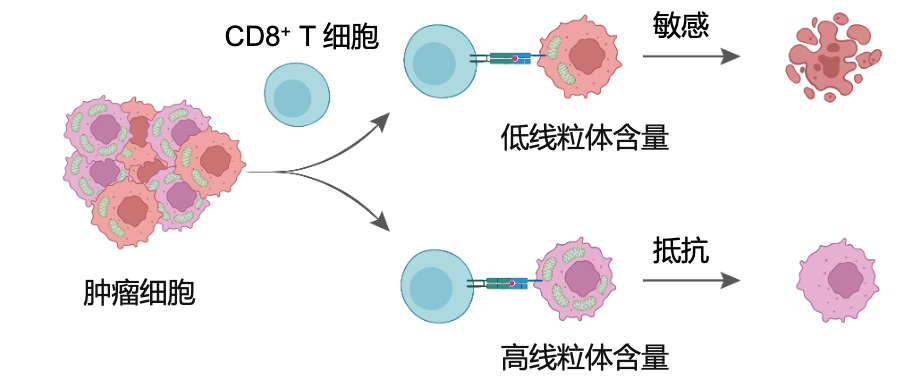
CD8+T更倾向于杀伤线粒体含量较低的肿瘤细胞
中国科学院国家纳米科学中心团队开发的mitoNIDs纳米降解剂,为解决这一难题提供了新思路。
其核心是“纳米诱导临近技术”:如同“牵线搭桥”,让原本距离较远的生物分子靠近以触发特定反应。
mitoNIDs由金纳米颗粒构成双功能系统,一端通过线粒体靶向肽精准定位癌细胞线粒体,另一端连接自噬相关蛋白LC3识别肽,诱导线粒体与自噬系统靠近,启动选择性自噬降解。
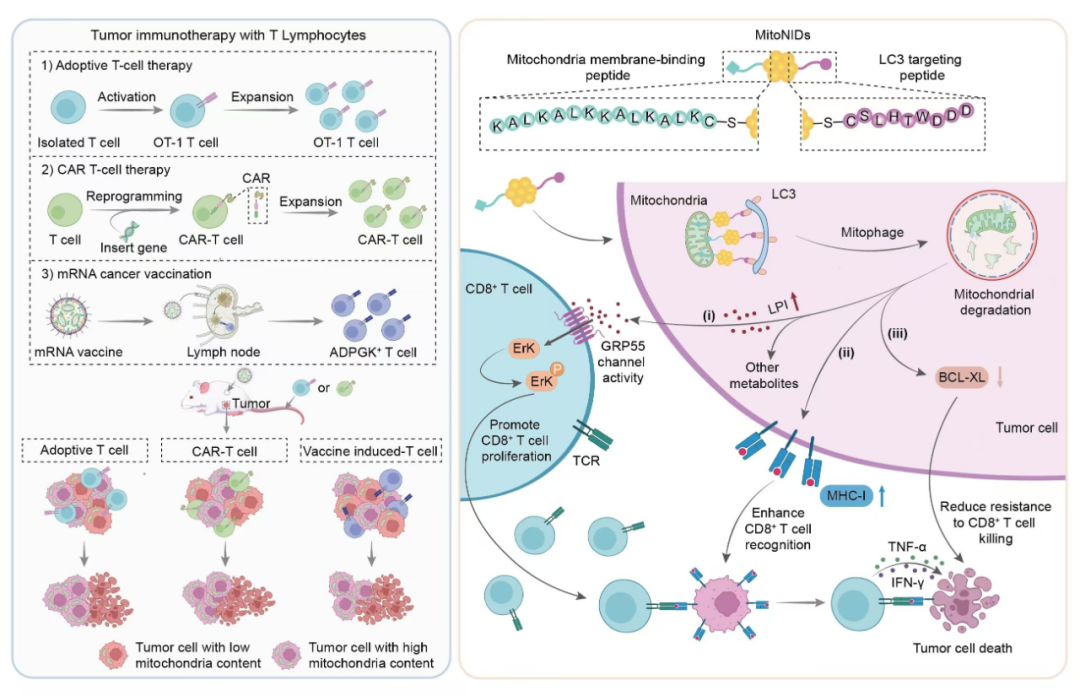
纳米诱导临近剂精准诱导肿瘤细胞“自毁线粒体”增效免疫治疗
线粒体被降解后,CD8+T细胞战斗力从三方面提升:肿瘤细胞表面MHC-I分子增多,更易被识别;抗凋亡蛋白BCL-XL减少,癌细胞更易被击杀;线粒体降解释放的信号分子溶血磷脂酰肌醇,能激活T细胞活性。
在小动物肿瘤模型中,mitoNIDs与免疫疗法联用已展现显著肿瘤抑制效果,后续需临床试验验证。
未来,这类纳米“牵线搭桥”工具或扩展至自身免疫病、神经退行性疾病等领域,助力人类在分子尺度精准干预生命过程。



