来源:雪球App,作者: nephroJin,(https://xueqiu.com/7875228039/300894794)
前言:
Adaptimmune获得FDA加速批准TECELRA®以后市场一片欢呼,但开盘当头一棒,股价从1.32暴跌至最低点0.94。
同时有TCR-T概念的香雪制药股价半个月三倍,可谓是出尽了风头。
ps:在这里我很好奇,加速审批什么时候变成获批上市了?

这种低级错误是在1w7粉丝的bio投资大v的专栏里能有的吗?@药时代

你自己贴的图都写了Accelerated啊?
anyway,我也在8月6日0.97的本少量买入参与这场“炒作”。

也希望各位能明白Car-T相关内容,这部分内容能让各位球友更好的理解Tcr-T
- Car-T、清淋治疗、细胞因子释放综合征和免疫效应细胞相关神经毒性综合征在【医药领域深度分析】Actinium v.2-Iomab管线(网页链接)详细讲解。这对理解为什么Tcr-T是革命性治疗手段尤为重要。
- CAR/TCR-T部分的基本内容在【JIN观医宏】靶向药/检查点抑制剂/癌症疫苗/ADC/RDC?一文讲清肿瘤治疗策略及未来研究方向里的癌症疫苗小结里。
(网页链接)
当然,废话到此为止。下面我会讲清Adaptimmune和香雪制药的Tcr-T。
CAR/TCR-T:
免疫疗法(Immunotherapy)大大改善了特定类型肿瘤患者的治疗效果。 越来越多的血液恶性肿瘤和实体瘤患者正在采用细胞疗法(ACT)-基因工程T细胞的治疗。 通过输注活体激活的自体或异体 T 细胞,同时使用或不使用其他抑制肿瘤微环境中 T 细胞的药物,ACT 可以克服目前某些免疫疗法的局限性。
目前正在开发的有两种通用的 ACT 方法。
- CAR-T使用嵌合抗原受体(Chimeric Antigen Receptor, CAR)使用引入免疫效应细胞的人工受体来识别肿瘤细胞表面蛋白。
-TCR-T 使用T细胞受体(T-cell Receptor, TCR)识别抗原。TCR通过识别由MHC分子呈递的肽抗原来激活T细胞反应。这意味着TCR-T细胞能够识别肿瘤细胞内的抗原,只要这些抗原能够被处理并由MHC展示出来。因此,TCR-T细胞可以识别更多样的抗原,尤其是那些来自细胞内部的抗原。
说白话就是CAR-T只能识别肿瘤细胞表面抗原,而TCR-T能识别肿瘤内部的抗原.
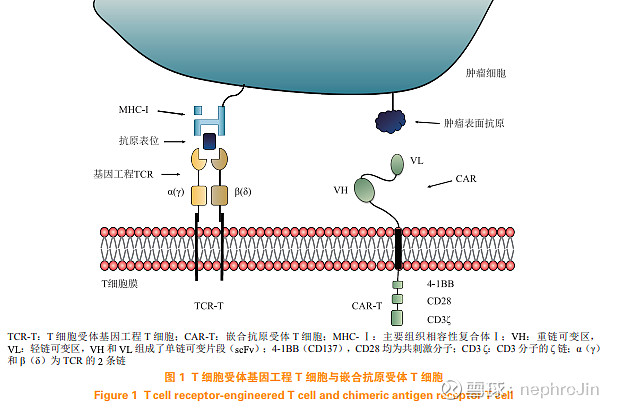
source:T 细胞受体基因工程 T 细胞治疗的现状与未来
那TCR-T怎么做到识别肿瘤内部的抗原呢?这必须得了解MHC和抗原递呈部分的内容.
MHC和抗原呈递
抗原加工和呈递是蛋白质抗原与自身 MHC 分子结合并呈递给具有适当受体的 T 细胞的过程。 它可分为两个部分;
抗原加工:它将大型抗原蛋白转化为短肽,与 MHC 分子(I 类或 II 类)一起显示在细胞膜上,并被 T 细胞识别。
抗原呈递:在这一过程中,人体内的某些细胞,尤其是抗原呈递细胞(APCs),会在细胞表面表达经过处理的抗原和MHC分子,并被T细胞识别。
CD8+ TC 细胞识别与 I 类 MHC 分子一起呈现的抗原,而与 II 类 MHC 分子一起呈现的抗原则由 CD4+ TH 细胞识别.
只要抗原被加工,并且被表面MHC分子所呈现,TCR-T就能识别此癌细胞.
因此CAR-T更适合血癌的治疗,而TCR-T适合实体瘤的治疗.
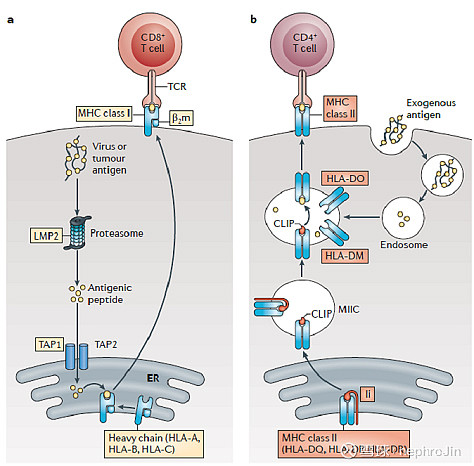
source:medicalbiochemist
TCR-T疗法流程
(1) 患者筛查从 HLA 分型开始。 如果 HLA 为 A*02:01 型,则进行肿瘤活检
(2)筛查肿瘤组织中目标抗原的表达
(3)进行白细胞分离
(4)从患者白细胞中分离出白细胞介质,并使用抗 CD3 和 CD28 抗体进行预激活
(5)从健康供体中分离出目标特异性 TCR,对其进行表征和修饰
(6)构建慢病毒载体,用于在 T 细胞中转导靶特异性 TCR
(7) 用编码目标特异性 TCR 的慢病毒载体转导活化的 PBMC
(8)转导的 T 细胞在 3-5 天内大量扩增并冷冻
(9)完成释放测试后,T 细胞就可以输注了
(10)先接受清林治疗,然后输注 T 细胞产品,最后注射低剂量白细胞介素,并对患者进行长达 15 年的监测,以观察患者在接触研究基因治疗产品后是否出现延迟不良反应。
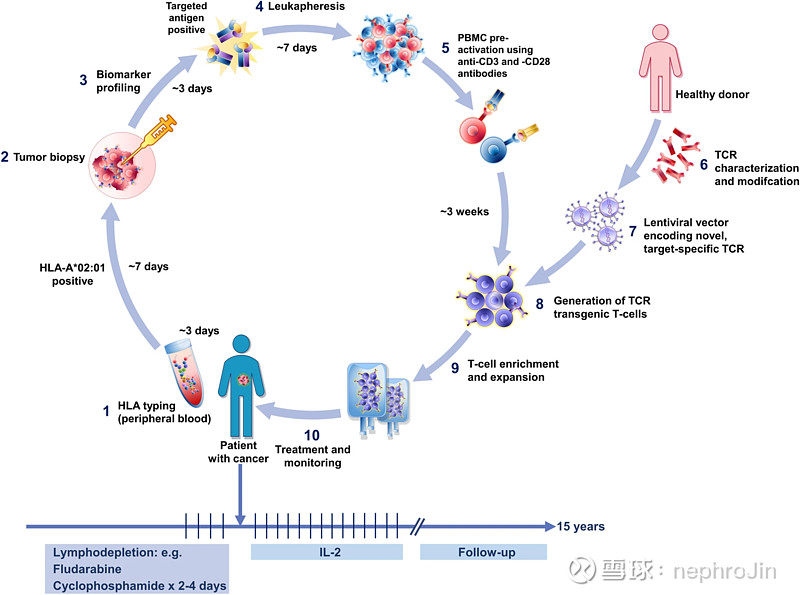
source:J Hematol Oncol.2021; 14: 102
Afami-cel(Adap)与TAEST16001(香雪)
上面讲了TCR-T的基本概念.那我们来讲讲Adaptimmune的Afami-cel和香雪制药的TAEST16001.
平台
首先必须得说明一点,就是香雪的TCR-T平台是Athenex的TAEST平台,这个平台怎么说呢…跟Adaptimmune的SPEAR平台比的话…在TCR亲和力优化、脱靶效应管理以及多抗原靶向方面具有较高的技术成熟度,存在一定劣势。(这部分非我擅长领域,我咨询了相关领域的资深研究员)
靶点
TAEST16001 针对的是HLA-A02:01 结合的 NY-ESO-1 抗原肽。
Afami-cel针对的是HLA-A*02:01 结合的 MAGE-A4 抗原肽.
我说实话TCR-T治疗机制有什么区别吗??我相信这位球友可能想表达的是针对“靶点”不同.

但据我了解在sarcoma中MAGE-A4表达率比NY-ESO-1高啊?
日本九州大学骨外科发表论文:通过免疫组化和实时聚合酶链反应分析了108个SSs中的MAGEA4和NY-ESO-1的表达。免疫组化结果显示,108 例 SS 中分别有MAGEA4 positibve 89 例(82%)和 NY-ESO-1 positive 66例(61%)…..

source:Kunio I et al.,Human Pathology.2017
来自于比利时的研究,探索了临床滑膜肉瘤队列中MAGE-A4和NY-ESO-1这两个基因的表达情况。通过来自91个患者的108个穿刺标本所构成的323孔的组织芯片进行检测。样本来源包括62%的原发肿瘤,22%的转移灶和16%的局部复发灶。NY-ESO-1和MAGE-A4 表达阳性分别占到了50.9%和68.5%,其中高表达分别占18.5%和23.1%。
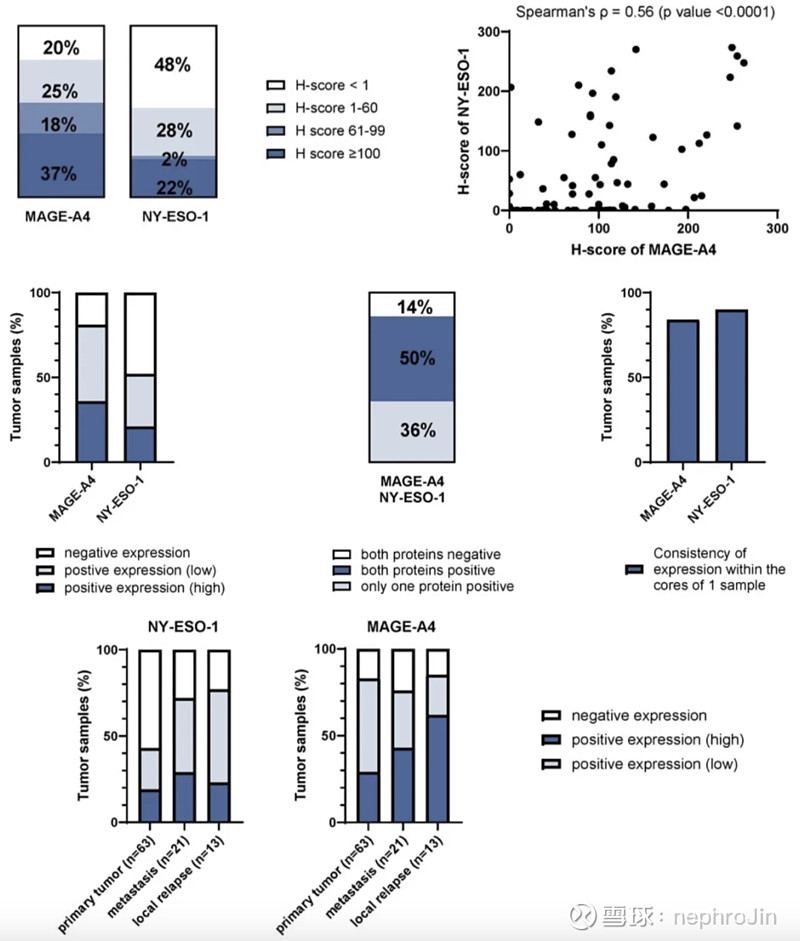
source:1953P Prognostic value of pretreatment inflammatory markers and other clinicopathological factors for early recurrence in soft tissue sarcoma
二期临床数据
这部分才是最令人诟病的.
TAEST16001的I期临床试验 12 名患者ORR 为 41.7%.
II期临床试验(NCT05549921)共入组8例患者,患者获得部分缓解(PR),37.5%(3例)患者达到病情稳定(SD)。客观缓解率(ORR)达到50%,远超出预先设定的目标缓解率(ORR=25%)。中位无进展生存期(PFS)为5.9个月。初始缓解中位时间达1.1个月(1.1~2.2),缓解持续时间的中位时间长达5.0个月(1.5~8.8)。
Afami-cel的I期临床试验 38名患者,结果发表到学术界顶刊nature.ORR24%.
II期临床试验44名患者,ORR 43%,其中CR 4.5%,中位数持续反应时间是6个月,对于响应治疗的病人,39%的病人响应时间是1年和以上。
学术造假
TAEST16001的一期二期总计20名患者,Afami-cel的一期二期总计82名患者.
2024年2月12日,《Nature》刊登了一篇题为《China conducts first nationwide review of retractions and research misconduct》的报道。文章指出,自2021年以来,全球范围内涉及中国学者的撤稿已超过17000篇,2023年全年撤稿论文中,约四分之三来自中国学者。
去年Hindawi撤回的论文数量超过9600篇,其中约有8200篇涉及中国学者。
因此平台落后,靶点并不优秀的TAEST16001拿出这么漂亮的成绩的时候,肯定是受到同行质疑的.
最后
其实不管是香雪也好ADAP也罢,不管是谁只要能继续推动TCR-T疗法,给绝望的患者带去阳光,都是值得被尊敬的.
但通过“筛选患者”,“数据美化”的方式进行圈钱的风气继续盛行下去,中国创新药永远都无法发展起来.
今天看@海上华尔兹 对A股医药给不了理智估值,只能炒垃圾而感慨.
但我还是希望ADAP能顺利通过FDA,也希望香雪在海外的临床试验也获得与中国开展一样的好结局,狠狠的打质疑者的脸.

