来源:雪球App,作者: nephroJin,(https://xueqiu.com/7875228039/299745301)

摘要
-癌症的本质是正常细胞的异常增殖和失控。
-癌症的基本特征包括抗凋亡、维持增殖信号、诱导血管生成和逃避宿主免疫监视。
-靶向药物是专门针对癌细胞中的特定分子或通路设计的药物,检查点抑制剂是解除对免疫细胞(主要是T细胞)的抑制作用,从而增强机体的抗肿瘤免疫反应。
-抗癌药物设计进入了新纪元,多靶点靶向药物、抗体药物偶联物和核素偶联药物代表了抗癌药物的未来竞争方向。
前言
创新药投资过程中最重要的主题之一便是“靶向药”。然而,目前尚无一篇文章能够系统地阐明靶向药、检查点抑制剂、抗体药物偶联物以及放射性药物偶联物之间的区别。许多投资者对上述药物存在混淆,甚至大多数投资者对肿瘤及其治疗手段的了解甚少。因此,我谨撰写此篇综述,旨在为投资者提供关于肿瘤治疗策略及未来研究方向的参考。
癌细胞-失控繁殖的“正常细胞”
癌症的本质是正常细胞的异常增殖和失控。正常细胞在体内有严格的生长、分裂和死亡的调控机制,而癌症细胞则因基因突变或其他因素导致这些机制失调,从而形成不受控制的增殖和生长。
癌症的分类
实体癌中,异常细胞会形成肿块或肿块块,称为肿瘤。
在骨髓癌中,异常细胞会在血液中积聚,称为白血病。
最先发生的癌症称为原发性癌症。 如果未扩散到身体其他部位,则被视为局部癌症。
良性肿瘤往往生长缓慢,通常不会转移到身体其他部位或转化为癌症。
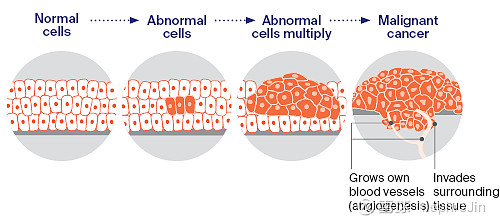
source:cancer concil
癌症的转移
恶性肿瘤具有侵袭性。它们可能会直接侵入附近的组织,破坏正常细胞.称为浸润性癌。 癌细胞脱落并通过血液(Blood)或淋巴管(Lymph vessel)转移到身体的其他部位,称为转移癌。

source:cancer concil
癌症的治疗
1. 外科手术: 通过手术切除肿瘤组织,但通常适用于早期和局限性肿瘤。
2. 放疗和化疗: 通过放射线或化学药物杀伤快速分裂的癌细胞,但也会对正常细胞造成损伤。
3. 靶向治疗: 通过靶向特定的癌症相关分子(如EGFR、HER2等)来干预癌细胞的生长和生存。
4. 免疫疗法: 包括检查点抑制剂(如PD-1/PD-L1抑制剂)、CAR-T细胞疗法、TCR-T细胞疗法等,通过增强免疫系统对癌细胞的识别和杀伤。
5. 精准放化疗: 包括抗体药物偶联物(ADC)、放射性药物偶联物(RDC)
6.其他: 激素治疗、干细胞移植、个性化定制基因治疗等。
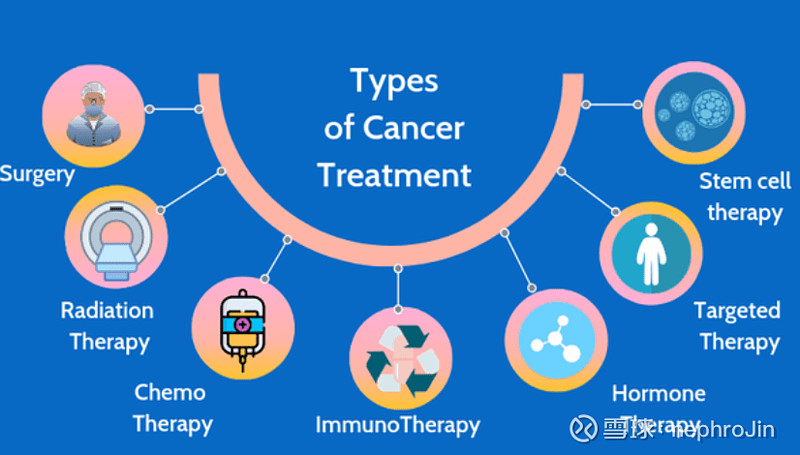
source:drsalunkhe
靶向药(target therapy)和检查点抑制剂(checkpoint inhibitor)的区别
谈药物之前,咱先把抗癌药物的设计思路先简单整理一下,这样更方便各位投资者的理解.
癌症的基本特征,包括抵抗凋亡、维持增殖信号、诱导血管生成和逃避宿主免疫监视。
靶向药物是专门针对癌细胞中的特定分子或通路设计的药物,旨在阻断这些分子的功能,从而抑制癌细胞的生长和扩散.也就是上述针对癌症的基本特征中的抗凋亡、维持增殖信号、诱导血管生成.
检查点抑制剂是通过阻断免疫系统中的“检查点”分子,解除对免疫细胞(主要是T细胞)的抑制作用,从而增强机体的抗肿瘤免疫反应。也就是癌症基本特征中的逃避宿主免疫监视。
下图为抑制肿瘤血管生成、过度生长和免疫逃避的主要分子靶向疗法类型概览,我将一个一个展开说明.
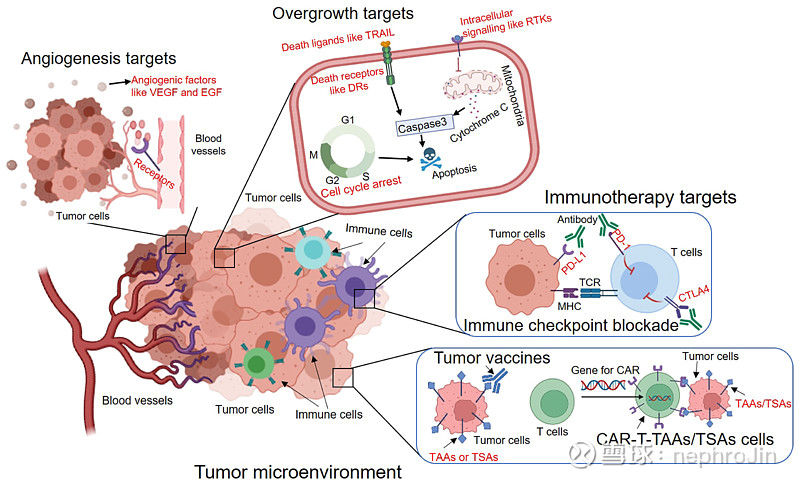
The overview of major types of molecular targeted therapies to inhibit tumour angiogenesis, overgrowth and immune evasion.
Source: Jue H et al., Front. 2022
靶向药
抗血管生成针对VEGFR和EGFR
针对VEGFR的靶向药物有贝伐珠单抗(Bevacizumab),阿昔替尼(Axitinib),雷莫芦单抗(Ramucirumab).适应症为结直肠癌、非小细胞肺癌、肾细胞癌等。针对EGFR靶向药物油吉非替尼(Gefitinib),厄洛替尼(Erlotinib),阿法替尼(Afatinib).适应症为非小细胞肺癌、头颈癌等。
诱导凋亡针对Trail/Drs或RTKs
靶向药物通过作用于特定的分子靶点,能够有效诱导癌细胞凋亡。
下图为TRAIL 对 DR4 和 DR5 的激活诱导外源性凋亡途径
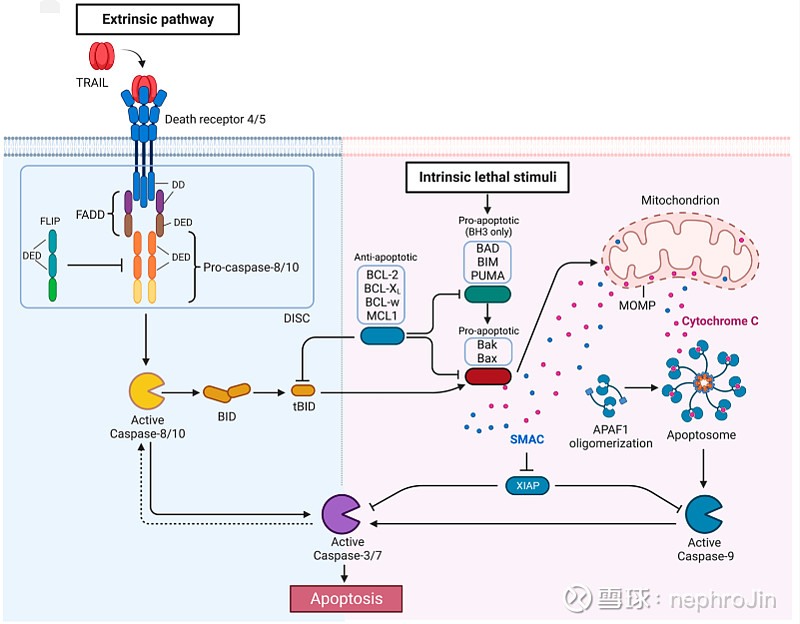
source:Manjari K.,MDPI.2022
Dulanermin(rhApo2L/TRAIL)是第一种同时结合DR4和DR5受体的促凋亡受体激动剂,触发外源性凋亡途径。
在临床前研究中,rhApo2L/TRAIL可选择性地触发癌症细胞的凋亡,且不伤害正常细胞。
一项针对晚期非小细胞肺癌(NSCLC)患者的 III 期临床试验中,Dulanermin与长春瑞滨和顺铂联合使用。结果表明,虽然杜拉奈明能显著改善无进展生存期(PFS),从3.5个月(安慰剂)提高到6.4个月,但并不能显著提高总生存期(OS)。
因此,尽管Dulanermin已完成 III 期试验并显示出一定的临床疗效,但由于药代动力学方面的挑战,其总体影响有限,基于 TRAIL 的疗法的进一步开发和优化仍在继续。
RTKs靶向药物,如上面提到的针对EGFR VEGFR的药物外还有HER2/neu抑制剂.
如曲妥珠单抗(Trastuzumab)能够与HER2受体结合,抑制其信号传导,诱导癌细胞凋亡。帕妥珠单抗(Pertuzumab)通过阻断HER2异二聚化,抑制癌细胞生长.
检查点抑制剂
目前,PD-1、PD-L1和CTLA-4是最常见和应用最广泛的检查点抑制剂靶点,相关药物已获批用于多种类型的癌症治疗。LAG-3、TIM-3、TIGIT等新兴靶点的研究正在进行中.
PD-1抑制剂(最经典的如O药 K药)可阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,释放PD-1信号通路介导的免疫反应抑制,从而激活可能影响肿瘤细胞和健康细胞的T淋巴细胞,进而增强人体免疫系统发现和消灭癌细胞的能力。
CTLA4:伊匹木单抗(又叫做Y药,唯一一款上市CTLA-4)是一种单克隆抗体,结合CTLA-4,阻断CTLA-4与其配体(CD80/CD86)结合,增加T细胞激活和增殖,包括肿瘤浸润性T细胞的激活和增殖。抑制CTLA-4传到信号可降低T调节细胞的功能,增加T细胞的表达,包括抗肿瘤免疫应答。
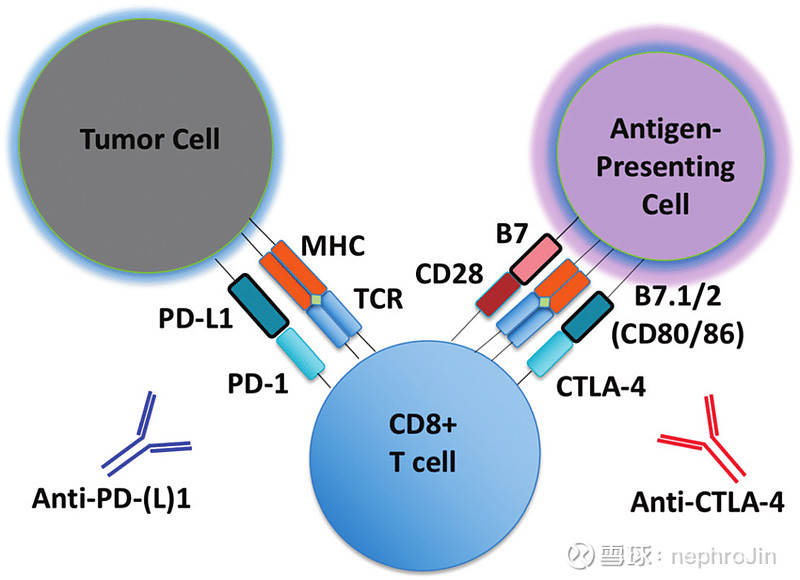
PD-1/CTLA-4 阻断示意图.
肿瘤相关抗原或新抗原通过 APC 或MHC呈现给具有TCR的 T 细胞.T 细胞上的 CD28 协同激活受体与 APC 上的 B7 结合。抗 PD-(L)1 和抗 CTLA-4 抗体的阻断位点.
source:Amir R Aref et al.,Lab chip.2018
癌症疫苗:CAR/TCR-T-TAAs/TSAs
肿瘤相关抗原(TAAs)和肿瘤特异性抗原(TSAs)通常用于癌症疫苗的开发,以激活机体的免疫系统攻击肿瘤细胞。
TAAs 是指在某些正常组织中低表达或在免疫豁免器官中表达,但在肿瘤中高表达的抗原。如癌睾丸抗原(cancer-testis antigen,CTA)、癌胚抗原(carcinoembryonic antigen,CEA)和组织分化抗原(tissue differentiation antigens,TDAs)等。
TSAs是由肿瘤细胞中的基因突变产生的新抗原,也被称为新生抗原(neoantigens)。这类抗原在正常组织中不存在,因此针对这类抗原的免疫治疗对正常组织的毒性很小。
CAR-T细胞疗法通过将患者的T细胞分离出来,并在体外通过基因工程手段将编码特定TAAs或者TSAs识别的嵌合抗原受体(CAR)的基因导入T细胞中,然后回输到患者体内。这些CAR-T细胞可以特异性识别和攻击表达特定TAAs/TSAs的肿瘤细胞。
TCR-T则是指将具有肿瘤抗原特异性的 TCR 通过基因工程技术导入到 T 细胞中,使 T 细胞获得识别和杀伤肿瘤细胞的功能。CAR-T 与 TCR-T 结构如图所示。
TCR-T目前也有一款药物获批上市:Tecelra-2024年8月1日,Adaptimmune旗下TCR-T疗法Afami-cel获FDA批准上市(首款获FDA批准上市的TCR-T药物),用于晚期滑膜肉瘤的治疗.
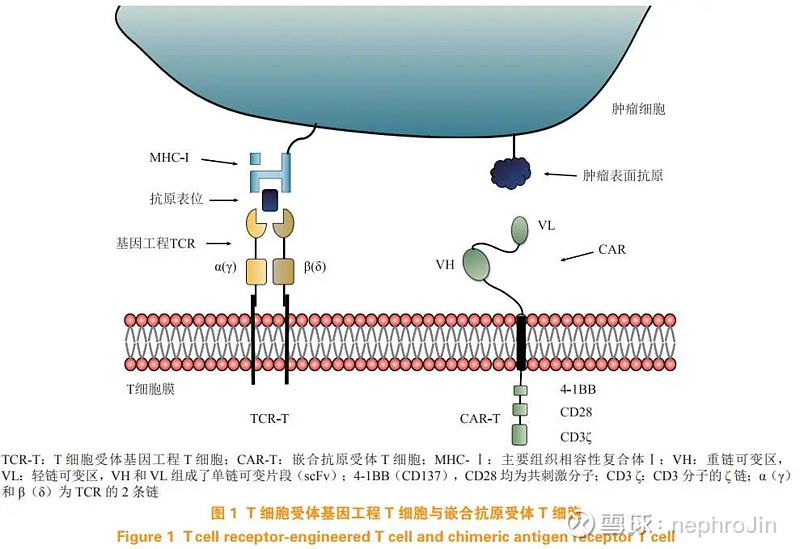
source:T 细胞受体基因工程 T 细胞治疗的现状与未来
以上是癌症治疗中最基本的理论知识,当把上述理论理解完成,才能明白接下来各大创新药企到底在哪些方面进行创新.
抗癌药物未来发展趋势
抗癌药物设计进入了新纪元,多靶点靶向药物、抗体药物偶联物(ADC)和核素偶联药物(RDC)代表了抗癌药物的未来竞争方向。它们各自通过不同的机制作用于癌细胞,提供了更为精准和有效的治疗手段。随着技术的发展和对癌症生物学理解的深入,这些药物的应用前景将更加广阔,为癌症患者带来更多的希望。
多靶点靶向药物
PD-1/VEGF双抗药物:AK112
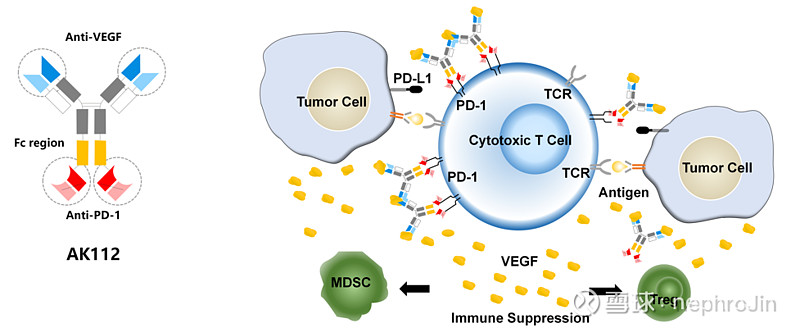
source:Akesobio
最近,康方生物的AK112在303试验中公布了首次中期分析结果,引起了广泛关注。该研究针对PD-L1表达阳性的非小细胞肺癌(NSCLC)患者进行了一线治疗的临床试验,直接与目前广泛使用的K药(Pembrolizumab)进行比较。结果显示,AK112在显著延长无进展生存期(PFS)方面表现出卓越的疗效。无论是PD-L1的表达水平、癌症类型(肺鳞癌或肺腺癌),还是患者的病情复杂程度(包括有无脑转移或肝转移),AK112在各个亚组中均展现了强阳性的PFS结果。
看完上面基础部分以后就可以理解AK112的设计结构了吧?
检查点抑制剂(PD1)+靶向药(抗VEGF)的结合体.
目前AK112已被中国获批上市.
抗体药物偶联物(ADC)
抗体药物共轭物(ADCs)是化疗药物+靶向药的结合体.利用抗体选择性地将细胞毒性药物输送到肿瘤部位,目前正处于快速发展阶段。迄今为止,共有 12 种 ADC 获得批准;, 它们是 Kadcyla、Adcetris、Besponsa、Mylotarg、Lumoxiti、Polivy、Padcev、 ;Trodelvy, Enhertu, Blenrep, ZYNLONTA ;and Tivdak.此外,目前有 80 多种 ADC 正在约 150 项活跃的临床试验中接受评估。
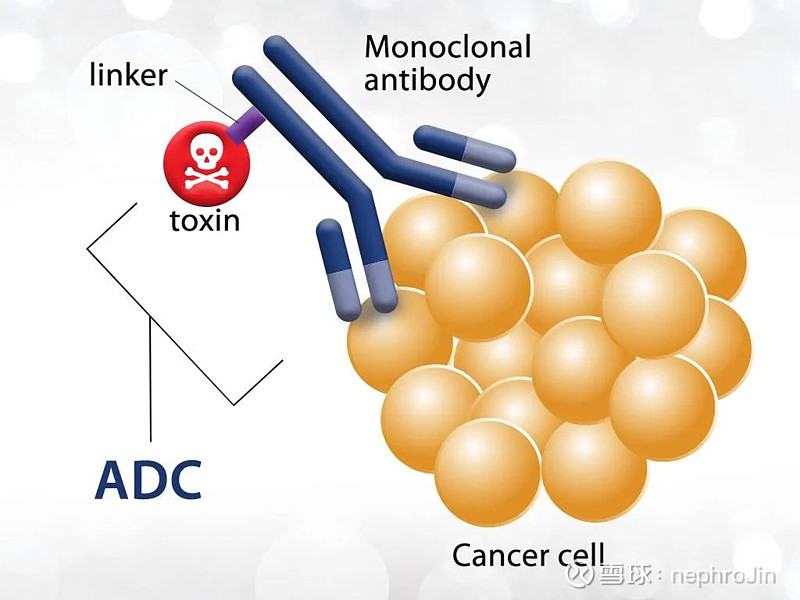
source:biochempeg
(HER2靶向药+细胞毒性药物)T-DXD:用于治疗HER2阳性癌症。T-DXd结合了单克隆抗体trastuzumab(HER2靶向药)和拓扑异构酶I抑制剂 (DXd) .
T-DXd通过结合HER2阳性的癌细胞表面受体,将deruxtecan直接递送到癌细胞内部。结合后的ADC通过内吞作用被癌细胞吸收,然后在细胞内释放出deruxtecan,干扰DNA复制过程,最终导致癌细胞死亡。
T-DXd在多项临床试验中展示出其显著的疗效和安全性。2022年6月ASCO大会上公布的亮眼数据,美国食品药品监督管理局(FDA)提前4个月批准了T-DXd的上市申请.不管是在HER2阳性还是HER2低表达的患者而言,T-DXd均可显著延长无进展生存期(PFS)和总生存期(OS).
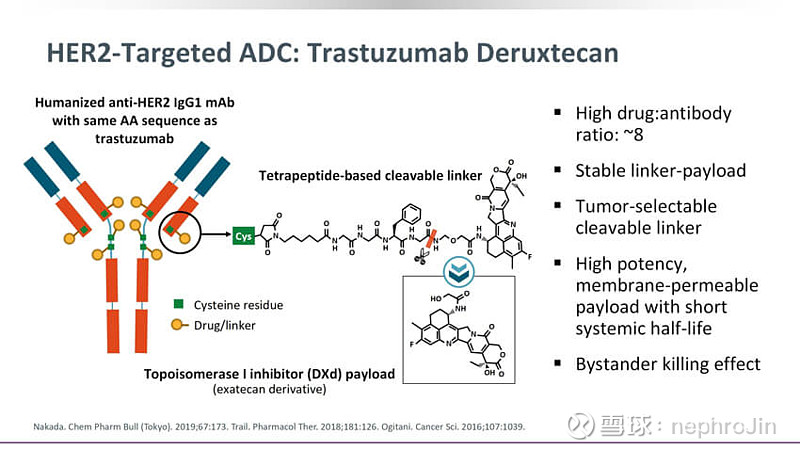
source:biochempeg
放射性药物偶联物(RDCs)
RDCs跟ADCs差不多,但是区别在于ADCs连接的是化疗药物,而RDCs连接的是放射性元素.如 I-131, Ac-225.
目前有比如Iomab-B等3期临床结果很好,等待申请BLA的药物.也有FPI-2265 针对三线+转移性抗性前列腺癌("mCRPC")的治疗的2期药物.
关于RDC我写的内容很详细,如有兴趣可移步以下链接:
详细阐述I-131的RDC在血液病中骨髓移植及癌症疫苗CAR-T使用过程中清淋步骤使用.
2.阿斯利康收购Fusion,精准核药领域又一家大鳄入局-网页链接
内容包括Fusion的Ac-225的RDC对前列腺癌的研究,及阿斯利康收购的意义.
总结:
肿瘤治疗领域的快速发展使得各类新型药物不断涌现,为患者提供了更精准和有效的治疗手段。在深入了解这些药物的作用机制和临床应用后,投资者可以更好地识别市场机遇,参与到未来的药物创新中。
最后,祝各位投资者投资顺利,收益丰厚!

