DRUGAI
今天为大家介绍的是来自复旦大学中山医院泌尿科郭剑明教授团队发表的一篇论文。在临床实践中,当医生意外发现患者的肾脏有肿块时,往往难以确定其性质,这给治疗方案的选择带来了挑战。要提供更精准的治疗方案,关键在于能够准确判断肿块是良性还是恶性,以及在恶性情况下肿瘤的危险程度。研究团队收集了4557名患者的13261份术前CT扫描影像,开发出两个基于人工智能的诊断模型。第一个模型用于判断肾脏肿块是否为恶性,其准确度(用AUC衡量)达到0.871,表现甚至超过了7位经验丰富的放射科医生。第二个模型则专门用来区分高危和低危的肿瘤,准确度达到0.783。这两个模型的表现都优于现有的医学影像分析方法。最重要的是,这项研究证明,通过分析术前的多阶段CT扫描图像,人工智能模型可以在不需要手术切片的情况下,准确预测肾脏肿块的性质和危险程度,为医生制定治疗方案提供重要参考。

随着医学影像技术的普及,医生能够更容易发现患者体内原本没有症状的肾脏肿块。然而,虽然手术治疗的数量在增加,但肾癌患者的死亡率并没有明显下降。这一现象提示我们,可能存在对良性肿块的过度治疗问题。研究发现,在所有被手术切除的肾脏肿块中,约有20%实际上是良性的。目前,医生主要通过CT和核磁共振检查来发现肾脏肿块,但这些方法难以准确判断肿块的性质和危险程度。虽然可以通过穿刺活检获取组织样本,但这种方法在20%的病例中无法得出明确诊断,而且有10%的诊断结果与手术后的最终病理结果不一致。
为了解决这个问题,研究团队开发了一种基于人工智能的诊断系统。这个系统通过分析患者的CT扫描图像,不仅能够区分良性和恶性肿块,还能判断恶性肿瘤的危险程度。与以往的人工智能模型相比,这个新系统的最大特点是考虑了更多类型的肾脏肿块,并通过分析肿瘤的多个特征(如生长方式、细胞特征等),更全面地评估肿瘤的危险程度。这种无创的诊断方法,有望帮助医生为患者选择更合适的治疗方案。
各研究组患者的筛选流程和临床特征
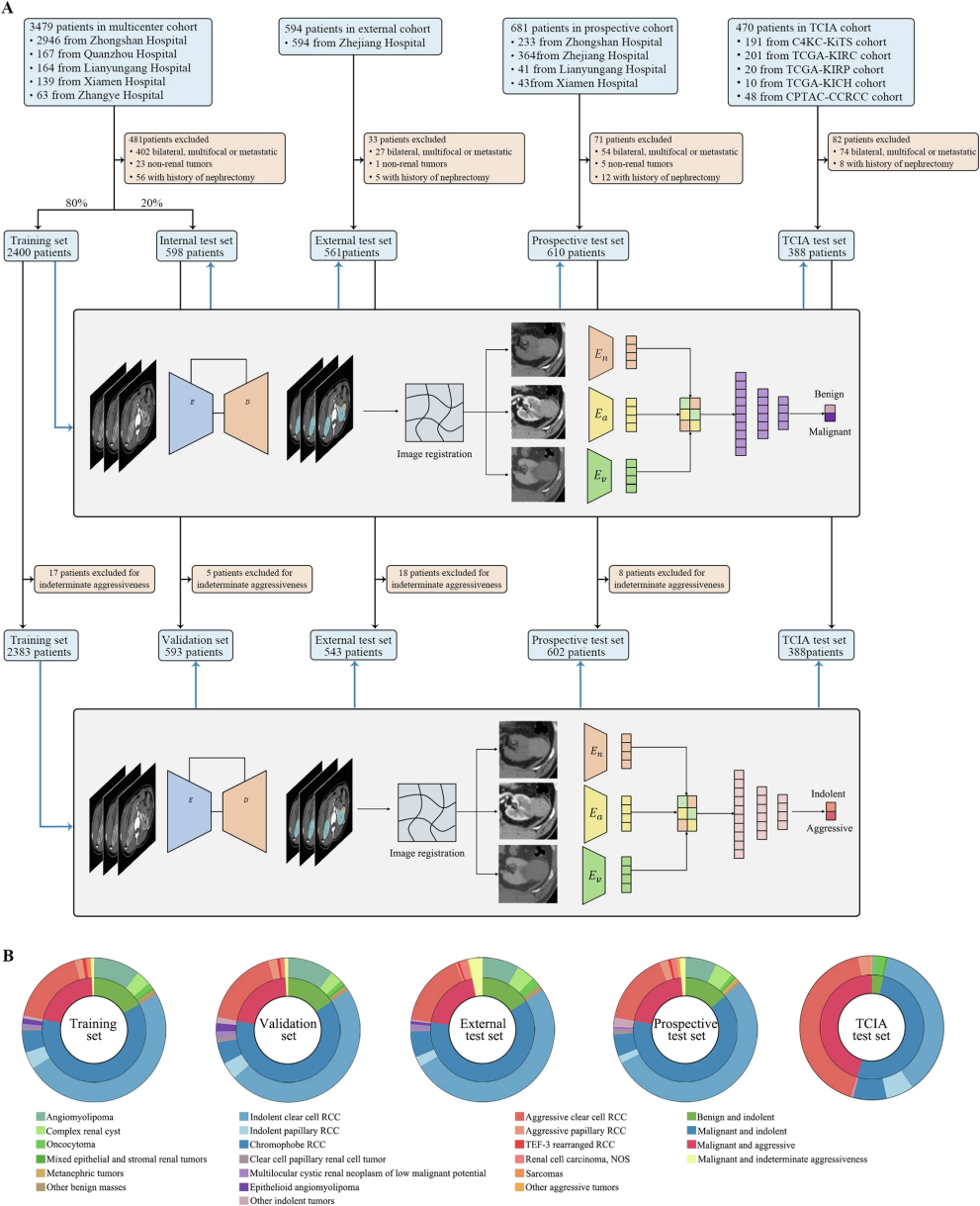
图 1
图1A展示了患者筛选和分组的详细过程。总共有4557名接受肾脏手术且进行过术前增强CT扫描的患者参与研究。这些患者被分为五组:训练集(2400人)、内部测试集(598人)、外部测试集(561人)、前瞻性测试集(610人)和TCIA测试集(388人)。研究将肾脏肿块分为三类:良性惰性型(对健康威胁较小)、恶性惰性型(虽为癌症但发展缓慢)和恶性侵袭性型(发展迅速需要及时治疗)。在大多数研究组中,这三类患者的比例相对稳定:良性惰性型约占15-17%,恶性惰性型约占61-63%,恶性侵袭性型约占20-21%。只有TCIA测试集的构成略有不同,其中恶性侵袭性型患者比例较高,达到45.4%。图1B则直观地展示了各组患者中不同类型肿瘤的具体分布情况,帮助我们更好地理解患者群体的构成特征。这种详细的分组数据为评估人工智能诊断模型的准确性提供了重要基础。
人工智能系统识别良性和恶性肾脏肿块的准确性评估
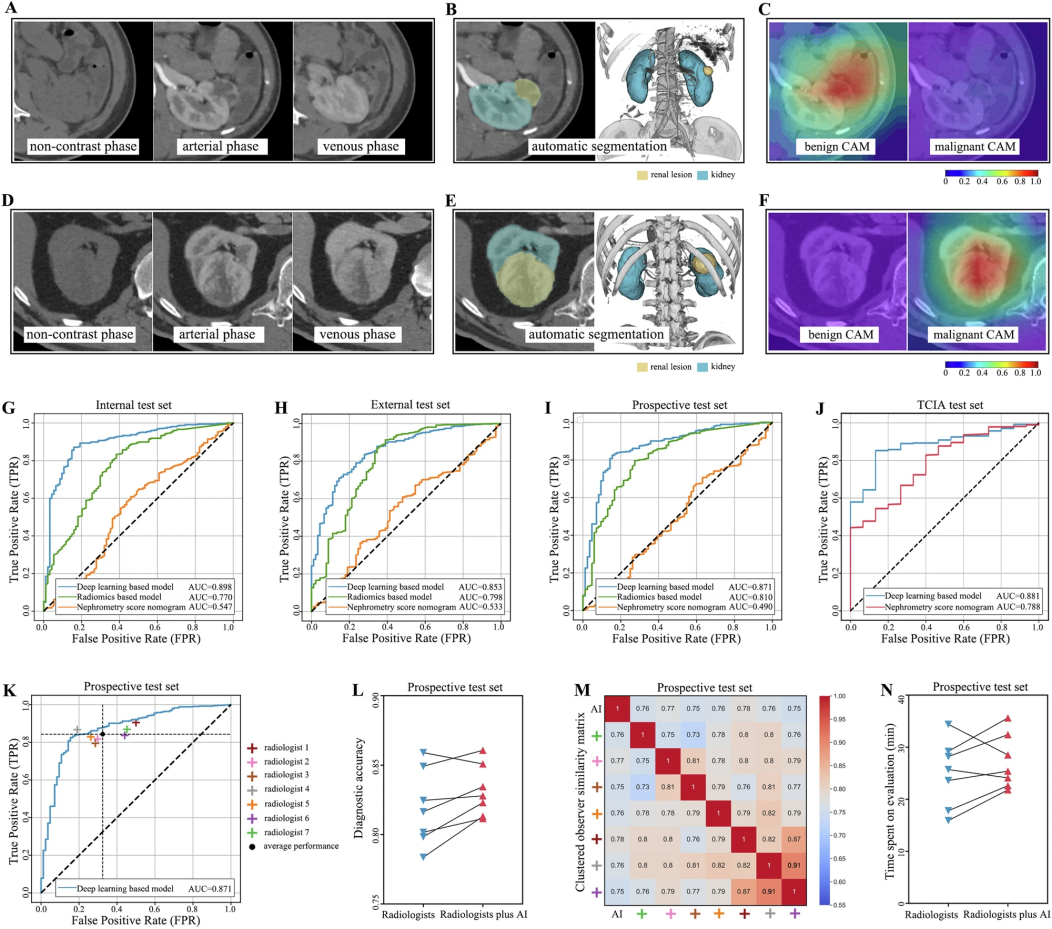
图 2
研究团队开发的人工智能系统在区分良性和恶性肾脏肿块方面展现出优异的表现。首先,AI系统能够准确识别和勾画出CT图像中的肾脏肿瘤区域,准确率达到85.2%。图2展示了两个典型案例:一个良性肾脏肿块(后肾腺瘤)和一个恶性肾脏肿块(透明细胞肾细胞癌)的CT图像。通过特殊的可视化技术,研究人员还能够直观地看到AI系统在做出判断时主要关注的图像区域。
在不同测试组中,该AI系统表现出很高的诊断准确性(用AUC值衡量,1表示完全准确):内部测试组达到0.898,外部测试组0.853,前瞻性测试组0.871,TCIA测试组0.881。这些结果都优于传统的评估方法。更令人印象深刻的是,研究团队邀请了7位经验丰富的放射科医生(每人都有超过5年的CT诊断经验)进行对比测试。结果显示,AI系统的表现超过了其中6位医生。有趣的是,当这些医生在两个月后重新进行诊断,并参考AI系统的预测结果时,他们的诊断准确率明显提高,而且诊断用时并没有增加。这说明AI系统不仅可以独立做出准确诊断,还能帮助医生提高诊断水平。这个AI系统在各种特殊情况下都表现稳定,无论是实体肿瘤、囊性肿瘤还是小型肾脏肿块,都能保持较高的诊断准确率。而且,它能够适应不同组合的CT扫描阶段,展现出很强的实用性。
人工智能系统在区分侵袭性和惰性肾脏肿瘤的诊断准确性
研究团队开发了第二个诊断模型来区分惰性(良性惰性和恶性惰性)和侵袭性(恶性侵袭性)肾脏肿瘤。为了验证这种分类方法的科学性,研究人员分析了来自中山医院和浙江医院的患者数据。结果显示,惰性肿瘤患者在疾病特异性生存期、无复发生存期和总体生存期等多个指标上都明显优于侵袭性肿瘤患者。
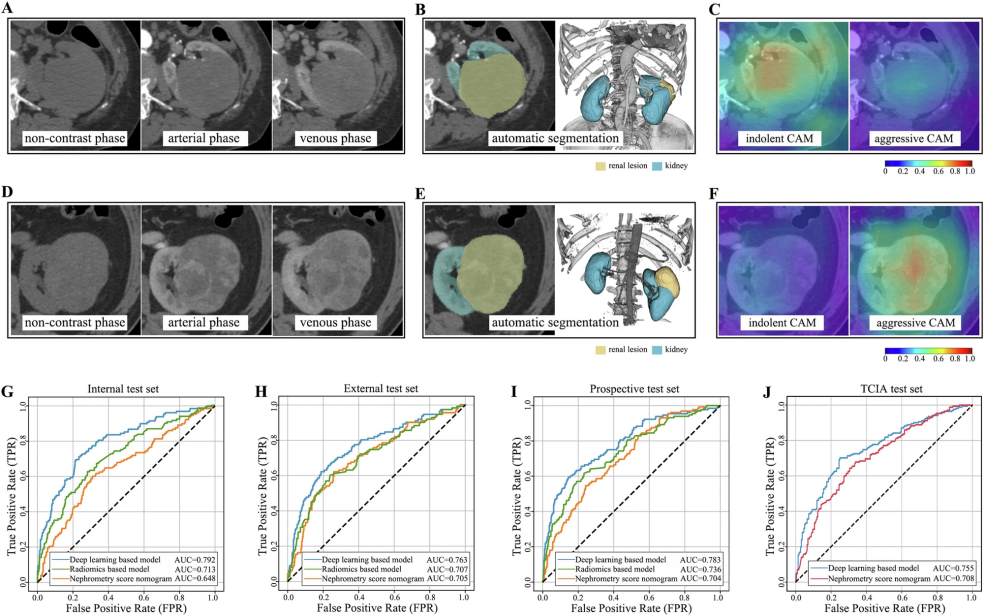
图 3
图3展示了两个典型病例的CT图像:上方是生长缓慢的惰性肾脏肿瘤(黏液性管状和梭形细胞肾细胞癌),下方是发展迅速的侵袭性肾脏肿瘤(未分类的肾细胞癌)。通过特殊的可视化技术,可以清楚地看到AI系统在判断肿瘤性质时重点关注的图像区域。这个AI系统在各类测试组中都表现出较高的诊断准确性:内部测试组达到0.792,外部测试组0.763,前瞻性测试组0.783,TCIA测试组0.755(数值越接近1表示准确性越高)。这些结果都优于传统的评估方法。更重要的是,无论面对实体肿瘤、囊性肿瘤还是小型肾脏肿瘤,AI系统都能保持稳定的诊断水平。这种全面的表现说明该系统在临床实践中具有广泛的应用前景。
影像学侵袭性与生存预后之间的关联
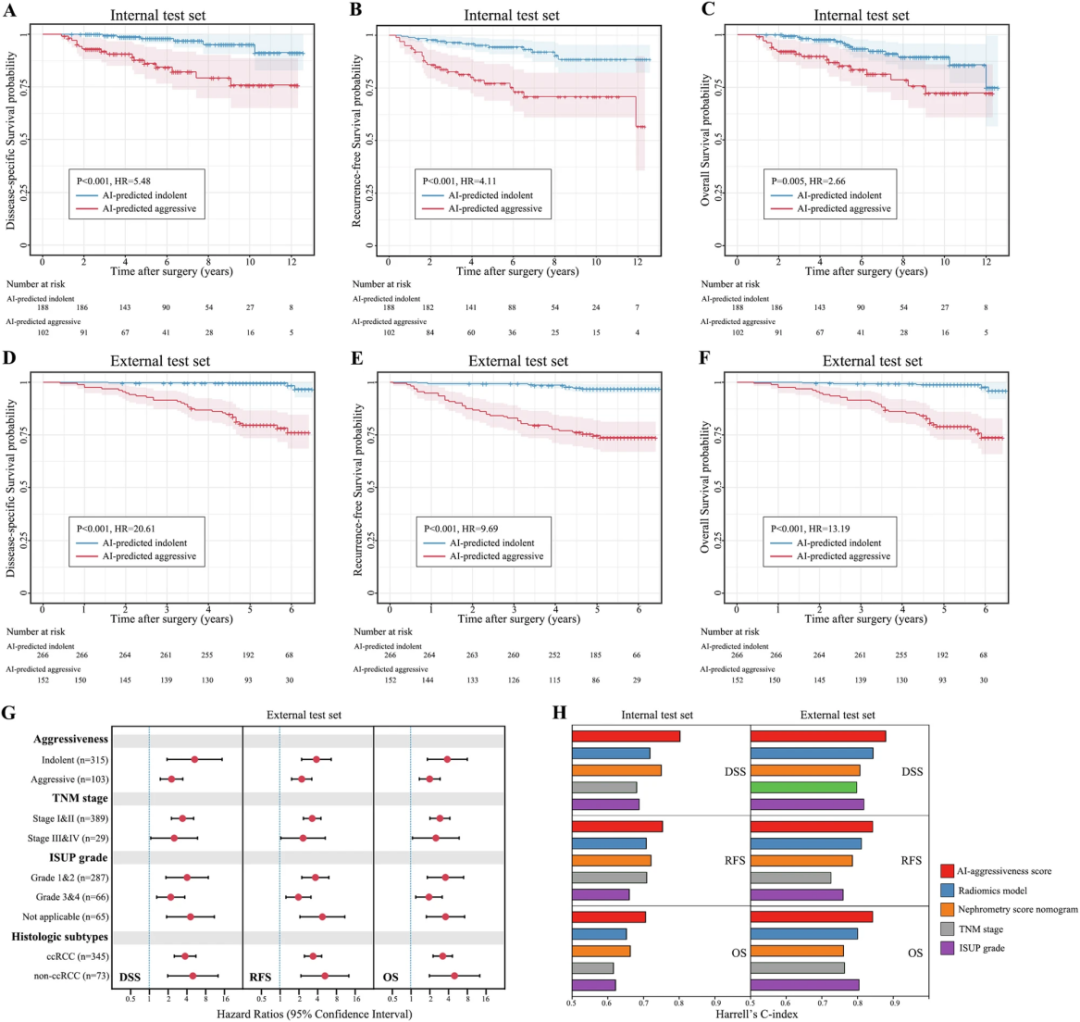
图 4
研究团队分析了AI预测的肿瘤侵袭性与患者生存结果之间的关联。图4A-F展示了在内部和外部测试集中,AI预测为惰性和侵袭性肿瘤患者的生存曲线对比。在内部测试集中,AI预测惰性肿瘤的5年生存率显著高于侵袭性肿瘤:疾病特异性生存率(97.9% vs 86%)、无复发生存率(94.5% vs 77.2%)和总体生存率(96.8% vs 85.1%)。
图4G的森林图显示,AI侵袭性评分在不同亚组(包括TNM分期、ISUP分级和组织学亚型)中都与患者预后显著相关。图4H比较了不同预后评估方法的预测价值,结果表明AI侵袭性评分在预测疾病特异性生存率、无复发生存率和总体生存率方面都优于其他风险评估方法。这些发现意味着,AI系统不仅能帮助医生更准确地判断肿瘤风险,还能为患者的治疗决策提供更可靠的参考依据。对于医生来说,这是一个强大的辅助工具;对于患者来说,这意味着可能获得更精准的治疗方案。
侵袭性和惰性肾脏肿瘤的基因和免疫特征差异
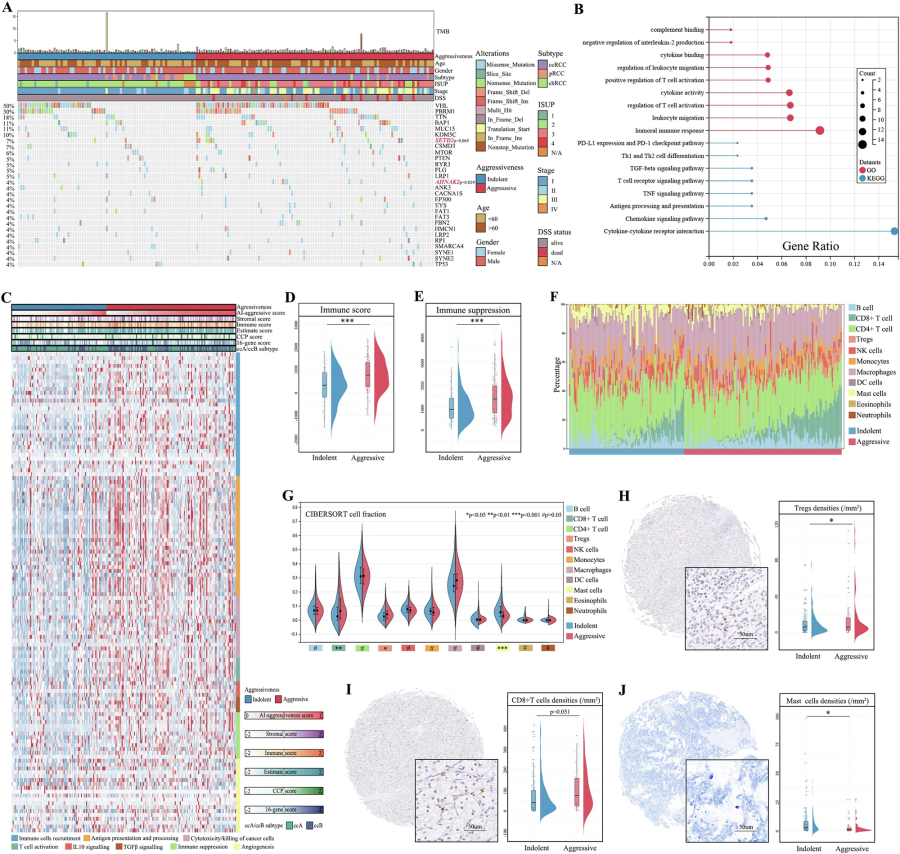
图 5
为了深入了解为什么某些肾脏肿瘤更具攻击性,研究团队从基因和免疫系统两个层面进行了探索。在基因层面,研究发现一个名为AHNAK2的基因在高危肿瘤中更容易发生突变(如图5A所示)。这个发现为理解肿瘤的侵袭性提供了新的线索。在免疫系统方面,研究团队分析了肿瘤周围的免疫环境(图5)。通过对229位患者的肿瘤组织样本进行特殊染色检查,发现:
高危肿瘤中含有更多的CD8+T细胞(一种重要的免疫细胞)和Tregs细胞(一种调节免疫反应的细胞);
低危肿瘤中则有更多的肥大细胞。
这些发现揭示了高危和低危肿瘤在微观层面的重要差异,有助于理解不同类型肿瘤的生物学特征,为未来开发更有针对性的治疗方法提供了方向。
讨论
随着医学影像技术的发展,医生能发现越来越多的肾脏肿块。但现有的诊断方法各有不足:活检会带来创伤和风险,单纯靠影像学检查又难以准确判断某些特殊类型的肿瘤。针对这一临床难题,研究团队开发了两个AI诊断系统:一个用来判断肿瘤是良性还是恶性,另一个用来评估肿瘤的危险程度。这些AI系统在多家医院的验证中都显示出优异的表现,不仅准确率超过了传统评分方法,还能辅助医生做出更准确的诊断。研究发现这种AI评估方法能有效预测患者预后,为临床治疗决策提供重要参考。
编译|于洲
审稿|王梓旭
参考资料
Xiong Y, Yao L, Lin J, et al. Artificial intelligence links CT images to pathologic features and survival outcomes of renal masses[J]. Nature Communications, 2025, 16(1): 1425.
内容中包含的图片若涉及版权问题,请及时与我们联系删除

